Ammoniumhydrogensulfat ist eine anorganisch-chemische Verbindung aus der Gruppe der der Hydrogensulfate; es handelt sich um das einbasische Ammoniumsalz der Schwefelsäure.
Bezeichnungen und Identifikatoren
Ammoniumhydrogensulfat
H5NO4S
(NH4)HSO4
115,103 (g/mol)
7803-63-6
232-265-5
BIGPRXCJEDHCLP-UHFFFAOYSA-N
Weitere Bezeichnungen, Synonyme
Ammoniumbisulfat; Schwefelsäure-Ammoniumsalz
Englische Bezeichnung
Ammonium hydrogen sulfate
Ammonium hydrogensulphate; Ammonium bisulfate; Sulfuric acid monoammonium salt
Chemische Formeln
Brutto- bzw. Summenformel und Strukturformel der chemischen Verbindung Ammoniumhydrogensulfat:
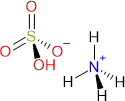
H5NO4S oder (NH4)HSO4
Mr = 115,103 g/mol
SMILES: [NH4+].OS(=O)(=O)[O-]
Daten und Eigenschaften
Übersicht über die (bekannten) chemischen und physikalischen Eigenschaften: Ammoniumhydrogensulfat. Es gelten - soweit nicht anders angegeben - Raumumgebungsbedingungen (Normaldruck, 0 % Luftfeuchtigkeit, 20 °C).
Ammoniumhydrogensulfat ist in reinem Zustand ein weißer, geruchloser, hygroskopischer Feststoff.
+ Leicht löslich in Wasser (> 1000 g/L bei 20 °C); löslich in Methanol.
- Unlöslich in Aceton.
120 °C
1,78 g cm-3 bei 20 °C
Spektroskopische Daten:
Prozentuale und isotopische Zusammensetzung:
Massenbezogene elementare Zusammensetzung und Isotopen-Anteile der Verbindung Ammoniumhydrogensulfat - H5NO4S - berechnet auf Grundlage der Molekülmasse.
.Element E
der Atome Ex
und der Isotope *
der Isotope
Ex an Formelmasse
Wasserstoff
ΣAr = 5,04 u
1H: 1,00783 u [99,99 %]
2H: 2,0141 u [0,01 %]
3H: 3,01605 u [<< 1 %]
1H: 4,37825 %
2H: 0,00044 %
3H: Spuren
Stickstoff
14N: 14,00307 u [99,6205 %]
15N: 15,00011 u [0,3795 %]
14N: 12,12292 %
15N: 0,04618 %
Sauerstoff
ΣAr = 63,996 u
16O: 15,99491 u [99,757 %]
17O: 16,99913 u [0,03835 %]
18O: 17,99916 u [0,205 %]
16O: 55,46379 %
17O: 0,02132 %
18O: 0,11398 %
Schwefel
32S: 31,97207 u [94,954 %]
33S: 32,97146 u [0,763 %]
34S: 33,96787 u [4,365 %]
35S: 34,96903 u [<< 1 %]
36S: 35,96708 u [0,016 %]
32S: 26,44784 %
33S: 0,21252 %
34S: 1,2158 %
35S: Spuren
36S: 0,00446 %
*) Die dritte Spalte führt die Atommassen bzw. Isotopenmassen der beteligten Elemente sowie - in eckigen Klammern - die natürliche Isotopenzusammensetzung auf.
Weitere berechnete Daten
Die molare Masse ist M = 115,103 Gramm pro Mol.
Die Stoffmenge von einem Kilogramm der Substanz ist n = 8,688 mol.
Die Stoffmenge von einem Gramm der Substanz ist n = 0,009 mol.
Monoisotopische Masse: 114,99392881475 Da - bezogen auf 1H514N16O432S.
Synthese, Gewinnung
Die direkte Umsetzung von Schwefelsäure und Ammoniak-Lösung liefert in erster Linie Ammoniumsulfat; die Halbneutralisation der Säure eignet sich daher nicht zur Darstellung von Ammoniumhydrogensulfat.
Man erhält das Salz in hoher Reinheit dagegen durch die Hydrolyse von Sulfaminsäure. Eine andere Möglichkeit ist die thermische Zersetzung von Ammoniumsulfat bei über 100 °C, wobei gasförmiges NH3 entweicht.
Große Mengen an Ammoniumhydrogensulfat entstehen als Abscheidungsprodukt in Aktivkoks-Filteranlagen für SO2-haltige industrielle Abgase.
Gefahren-Hinweise nach GHS
(Allgemeine Hinweise ohne Gewähr auf Richtigkeit und Vollständigkeit! Die Angaben ersetzen weder das Sicherheitsdatenblatt Chemikalien noch eine Gefährdungsbeurteilung, sondern geben eine allgemeine Übersicht hinsichtlich der Gefährdung durch den Gefahrstoff.)

Signalwort: Gefahr
Gefahrenhinweise (H-Sätze):
- H314
Verursacht schwere Verätzungen der Haut und schwere Augenschäden. - H318
Verursacht schwere Augenschäden.
Zur Kennzeichnung in der EU siehe ECHA Substance Infocard 100.029.332 sowie Informationen zu REACh unter ECHA Chem 100.029.332.
Zur Toxikologie und zum Arbeitsschutz beim Umgang mit Ammoniumhydrogensulfat sowie Maßnahmen im Gefahrenfall siehe: Gefahrstoffinformationssystem GESTIS, ZVG-Nr. 004300.
Beförderung gefährlicher Güter (Gefahrgut-Kennzeichnung): UN-Nummer 2506.
Externe Informationsquellen
Hersteller und Bezugsquellen
In der nachfolgenden Tabelle sind Produzenten und Lieferanten von Ammoniumhydrogensulfat als kommerzielle Chemikalie für Labor, Forschung, Industrie und Produktion mit den entsprechenden Kontaktdaten verzeichnet.
Literatur und Quellen
[0] - Fach- und Forschungsartikel in wissenschaftlichen Zeitschriften via PubMed: Ammonium_hydrogen_sulfate.
Letzte Änderung am 28.04.2024.
Permalink: https://www.internetchemie.info/substanz/Ammoniumhydrogensulfat.php
© 1996 - 2026 Internetchemie ChemLin