Bereits seit Jahrhunderten nutzen Menschen die Inhaltsstoffe von Pflanzen als Wirkstoffe in der traditionellen Heilkunde.
In den vergangenen zwanzig Jahren hat eine neuartige Klasse von Naturstoffen zunehmend für Aufmerksamkeit gesorgt: die polyprenylierten, polycyclischen Acylphloroglucine, kurz PPAP. Ihnen wurde nachgewiesen, unter anderem Mikroben den Garaus zu machen oder das unkontrollierte Wuchern von Krebszellen zu stoppen.
In einer Vorab-Onlinepublikation der Zeitschrift Nature Chemistry vom 16. Oktober 2011 [siehe unten] berichtet die Arbeitsgruppe um Prof. Bernd Plietker vom Institut für Organische Chemie der Universität Stuttgart, dass es ihr gelungen sei, in nur sieben aufeinander aufbauenden Reaktionen unterschiedlichste Vertreter dieser Naturstoffklasse in größeren Mengen selektiv herzustellen.
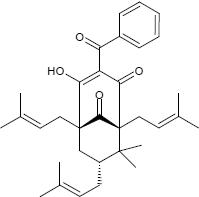
Mehr als 100 Vertreter aus der Naturstoffklasse der PPAP sind bereits bekannt. Die meisten davon wurden aus verschiedenen Pflanzen- und Baumarten der Familie der Clusiaceae isoliert. Sie sind strukturell sehr ähnlich und zeichnen sich durch ein gemeinsames Kohlenstoffgrundgerüst aus, an das fünf unterschiedliche Kohlenstoffseitenketten gebunden sind. Dabei scheinen ausschließlich die Kohlenstoffseitenketten für die exakte biologische Aktivität verantwortlich zu sein. "Insofern stellt das Grundgerüst der PPAPs eine neuartige, aus der Natur abgeleitete Leitstruktur dar, die unter Umständen der Wirkstrukturfindung und -optimierung in der pharmazeutischen Industrie neue Impulse geben könnte", begründet Plietker das Interesse von Chemikern, Biologen, Pharmazeuten und Medizinern an diesen Pflanzenstoffen. "Um die Forschung jedoch sinnvoll durchführen zu können, ist die Ausarbeitung eines Synthesewegs zur Herstellung natürlicher als auch nicht-natürlicher PPAPs eine Grundvoraussetzung", erklärt Plietker.
Die Chemiker am Institut für Organische Chemie konnten erstmals fünf vollkommen unterschiedliche Vertreter diese Naturstoffklasse mit nur wenigen Reaktionsschritten synthetisieren. Dabei erzielten sie Gesamtausbeuten von sechs bis 24 Prozent. Die Effizienz der PPAP-Synthese haben sie maximiert, indem sie diejenigen Reaktionen, die dem Gerüstaufbau dienten, von denjenigen Reaktionen getrennt haben, durch welche die Kohlenstoffseitenketten eingeführt werden. Dadurch können zukünftig sowohl die über 100 natürlichen PPAP-Vertreter größtenteils synthetisiert werden als auch nicht-natürliche PPAPs. Darüber hinaus haben Plietker und seine Mitarbeiter bei der Entwicklung des Syntheseweges darauf geachtet, dass dafür keine toxischen Reagenzien verwendet werden. Die direkten Abfallprodukte sind kleine Mengen nicht-toxischer Metalle sowie Alkohol, Wasser und Kohlendioxid.
Diese Entwicklung, so Plietker, könnte die Tür zu einer verstärkten Erforschung der Naturstoffklasse der polyprenylierten, polycyclischen Acylphloroglucine aufstoßen.
Vielleicht entstehen, basierend auf dieser Forschung, eines Tages neue und wirksamere Arzneimittel.
Zusatzinformationen:
Nicole Biber, Katrin Möws und Bernd Plietker:
The total synthesis of hyperpapuanone, hyperibone L, epi-clusianone and oblongifolin A.
In: Nature Chemistry; online veröffentlicht am 16. Oktober 2011, DOI 10.1038/nchem.1170
Quelle: Universität Stuttgart
Aktualisiert am 17.10.2011.
Permalink: https://www.internetchemie.info/news/2011/oct11/ppap-totalsynthese.php
© 1996 - 2026 Internetchemie ChemLin