Bleiwasserstoff ist eine binäre anorganische Verbindung aus der Gruppe der Stammhydride bzw. der Metallhydride, die chemisch auch als Plumban bezeichnet wird. Die unter Standardbedingungen gasförmige, sehr giftige Substanz besteht aus den Elementen Blei und Wasserstoff mit einem zentralen, vierwertigen Pb-Atom, an das vier H-Atome gebunden sind.
Bezeichnungen und Identifikatoren
Bleiwasserstoff
H4Pb
PbH4
211,232 (g/mol)
15875-18-0
XRCKXJLUPOKIPF-UHFFFAOYSA-N
Systematischer Name
Plumban
Weitere Bezeichnungen, Synonyme
Tetrahydridoblei; Blei(IV)-hydrid; Monoplumban
Englische Bezeichnung
Plumbane
Tetrahydridolead; Lead hydride; Plumbylidyne; Lead tetrahydride; Lead(IV) hydride
Chemische Formeln
Brutto- bzw. Summenformel und Strukturformel der chemischen Verbindung Bleiwasserstoff:
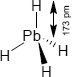
H4Pb oder PbH4
Mr = 211,232 g/mol
Plumban
SMILES: [PbH4]
Daten und Eigenschaften
Übersicht über die (bekannten) chemischen und physikalischen Eigenschaften: Bleiwasserstoff. Es gelten - soweit nicht anders angegeben - Raumumgebungsbedingungen (Normaldruck, 0 % Luftfeuchtigkeit, 20 °C).
Die farblose Blei-Verbindung wurde bisher kaum chemisch oder physikalisch charakterisiert. Das Molekül des Bleiwasserstoffs hat eine tetraedrische Struktur mit einem Gleichgewichtsabstand zwischen Pb- und H-Atom von 173 pm. Die formalen Oxidationsstufen von Wasserstoff und Blei sind +1 bzw. -4, da die Elektronegativität von Blei(IV) höher ist als die von Wasserstoff.
-13 °C
Spektroskopische Daten:
splash10-00di-0090000000-b3260214622e93116728
Prozentuale und isotopische Zusammensetzung:
Massenbezogene elementare Zusammensetzung und Isotopen-Anteile der Verbindung Bleiwasserstoff - H4Pb - berechnet auf Grundlage der Molekülmasse.
.Element E
der Atome Ex
und der Isotope *
der Isotope
Ex an Formelmasse
Wasserstoff
ΣAr = 4,032 u
1H: 1,00783 u [99,99 %]
2H: 2,0141 u [0,01 %]
3H: 3,01605 u [<< 1 %]
1H: 1,90861 %
2H: 0,00019 %
3H: Spuren
Blei
204Pb: 203,97304 u [1,4 %]
206Pb: 205,97447 u [24,1 %]
207Pb: 206,9759 u [22,1 %]
208Pb: 207,97665 u [52,4 %]
204Pb: 1,37328 %
206Pb: 23,63998 %
207Pb: 21,67815 %
208Pb: 51,39979 %
*) Die dritte Spalte führt die Atommassen bzw. Isotopenmassen der beteligten Elemente sowie - in eckigen Klammern - die natürliche Isotopenzusammensetzung auf.
Weitere berechnete Daten
Die molare Masse ist M = 211,232 Gramm pro Mol.
Die Stoffmenge von einem Kilogramm der Substanz ist n = 4,734 mol.
Die Stoffmenge von einem Gramm der Substanz ist n = 0,005 mol.
Monoisotopische Masse: 212,0079531288 Da - bezogen auf 1H4208Pb.
Synthese, Gewinnung
Die Stabilität von Metallhydriden mit der Formel MH4 nimmt mit steigender Ordnungszahl von M ab. Bleiwasserstoff ist thermodynamisch instabil und kann nicht mit den gleichen Methoden wie die leichteren Kongenere Silan, German und Stannan synthetisiert werden. Insgesamt handelt es sich um eine endotherme Verbindung
PbH4 ⇌ Pb + 2 H2 + 278 kJ,
die aus den Elementen nur mit atomarem (z. B. kathodisch erzeugtem) bzw. naszierendem Wasserstoff (Status nascendi) auf fein verteiltes Bleipulver zugänglich ist.
2003 untersuchten Wang und Andrews die Herstellung von Plumban durch Laser-Ablation und identifizierten die Substanz durch IR-Banden (PbH-Streckschwingung bei 1815,0 cm-1).
Gefahren-Hinweise nach GHS
(Allgemeine Hinweise ohne Gewähr auf Richtigkeit und Vollständigkeit! Die Angaben ersetzen weder das Sicherheitsdatenblatt Chemikalien noch eine Gefährdungsbeurteilung, sondern geben eine allgemeine Übersicht hinsichtlich der Gefährdung durch den Gefahrstoff.)



Signalwort: Gefahr
Gefahrenhinweise (H-Sätze):
- H302
Gesundheitsschädlich bei Verschlucken. - H332
Gesundheitsschädlich bei Einatmen. - H360Df
Kann das Kind im Mutterleib schädigen. Kann vermutlich die Fruchtbarkeit beeinträchtigen. - H400
Sehr giftig für Wasserorganismen. - H410
Sehr giftig für Wasserorganismen, mit langfristiger Wirkung.
Fortpflanzungsgefährdend (R).
Zur Kennzeichnung in der EU siehe ECHA Substance Infocard 100.290.477 sowie Informationen zu REACh unter ECHA Chem 100.290.477.
Externe Informationsquellen
Hersteller und Bezugsquellen
In der nachfolgenden Tabelle sind Produzenten und Lieferanten von Bleiwasserstoff als kommerzielle Chemikalie für Labor, Forschung, Industrie und Produktion mit den entsprechenden Kontaktdaten verzeichnet.
Literatur und Quellen
[1] - Fritz Paneth, Otto Nörring:
Über Bleiwasserstoff.
In: Berichte der deutschen chemischen Gesellschaft, (1920), DOI 10.1002/cber.19200530915.
[2] - Xuefeng Wang, Lester Andrews:
Infrared Spectra of Group 14 Hydrides in Solid Hydrogen: Experimental Observation of PbH4, Pb2H2, and Pb2H4.
In: Journal of the American Chemical Society, (2003), DOI 10.1021/ja029862l.
[3] - Bole Chen, Lewis J. Conway, Weiguo Sun, Xiaoyu Kuang, Cheng Lu, Andreas Hermann:
Phase stability and superconductivity of lead hydrides at high pressure.
In: Physical Review B, (2021), DOI 10.1103/PhysRevB.103.035131.
Letzte Änderung am 13.02.2024.
Permalink: https://www.internetchemie.info/substanz/Bleiwasserstoff.php
© 1996 - 2026 Internetchemie ChemLin