Bleicarbonat ist eine anorganische Verbindung, die chemisch als das Salz des zweiwertigen Schwermetalls Blei und der Kohlensäure beschrieben wird.
Bezeichnungen und Identifikatoren
Bleicarbonat
CO3Pb
PbCO3
267,208 (g/mol)
598-63-0
209-943-4
MFEVGQHCNVXMER-UHFFFAOYSA-L
Systematischer Name
Blei(II)-carbonat
Weitere Bezeichnungen, Synonyme
Kohlensaures Blei; Bleikarbonat; Blei(II)-karbonat
Englische Bezeichnung
Lead carbonate
Lead(II) carbonate
Chemische Formeln
Brutto- bzw. Summenformel und Strukturformel der chemischen Verbindung Bleicarbonat:
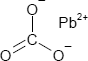
CO3Pb oder PbCO3
Mr = 267,208 g/mol
Blei(II)-carbonat
SMILES: C(=O)([O-])[O-].[Pb+2]
Daten und Eigenschaften
Übersicht über die (bekannten) chemischen und physikalischen Eigenschaften: Bleicarbonat. Es gelten - soweit nicht anders angegeben - Raumumgebungsbedingungen (Normaldruck, 0 % Luftfeuchtigkeit, 20 °C).
Blei(II)-carbonat liegt in reiner Form als weißer Feststoff bzw. als weißes Pulver vor, das praktisch unlöslich in Wasser ist.
315 °C
6,582 g cm-1 bei 20 °C
nD = 1,804
-61,2 × 10-6 cm3 mol-1
Wie andere Metallcarbonate auch nimmt Blei(II)-carbonat eine dichte, hochvernetzte Struktur an, die aus CO32- und Metallkationenzentren besteht. Durch Röntgenkristallographie wurde bestätigt, dass die Pb(II)-Zentren siebenfach koordiniert und von mehreren Carbonatliganden umgeben sind. Die Carbonatzentren sind zweizähnig an ein einzelnes Pb-Atom gebunden und überbrücken zu fünf anderen Pb-Stellen [1].
Raumgruppe Pmcn, Nr. 62, mit den Gitterkonstanten a = 517,9 pm; b = 849,2 pm; c = 614,1 pm, den Winkeln α = β = γ = 90 °, Z = 4.
Spektroskopische Daten:
Prozentuale und isotopische Zusammensetzung:
Massenbezogene elementare Zusammensetzung und Isotopen-Anteile der Verbindung Bleicarbonat - CO3Pb - berechnet auf Grundlage der Molekülmasse.
.Element E
der Atome Ex
und der Isotope *
der Isotope
Ex an Formelmasse
Kohlenstoff
12C: 12 u [98,94 %]
13C: 13,00335 u [1,06 %]
14C: 14,00324 u [<< 1 %]
12C: 4,44735 %
13C: 0,04765 %
14C: Spuren
Sauerstoff
ΣAr = 47,997 u
16O: 15,99491 u [99,757 %]
17O: 16,99913 u [0,03835 %]
18O: 17,99916 u [0,205 %]
16O: 17,91876 %
17O: 0,00689 %
18O: 0,03682 %
Blei
204Pb: 203,97304 u [1,4 %]
206Pb: 205,97447 u [24,1 %]
207Pb: 206,9759 u [22,1 %]
208Pb: 207,97665 u [52,4 %]
204Pb: 1,0856 %
206Pb: 18,68776 %
207Pb: 17,13691 %
208Pb: 40,63232 %
*) Die dritte Spalte führt die Atommassen bzw. Isotopenmassen der beteligten Elemente sowie - in eckigen Klammern - die natürliche Isotopenzusammensetzung auf.
Weitere berechnete Daten
Die molare Masse ist M = 267,208 Gramm pro Mol.
Die Stoffmenge von einem Kilogramm der Substanz ist n = 3,742 mol.
Die Stoffmenge von einem Gramm der Substanz ist n = 0,004 mol.
Monoisotopische Masse: 267,961396857 Da - bezogen auf 12C16O3208Pb.
Vorkommen
Blei(II)-carbonat kommt in der Natur als Mineral Cerussit vor, das auch Weißbleierz, weißer Bleispat und (historisch) Bleispath oder Bleiweiß genannt wird und verschiedene Verunreinigungen enthält.
Synthese, Gewinnung
Die Herstellung von Bleicarbonat erfolgt durch Einleitung von Kohlendioxid in eine kalte (10 °C) verdünnte Lösung von Bleiacetat, wobei das Bleisalz ausfällt. Die Umsetzung bei niedriger Temperatur unterdrückt die Bildung von basischem Bleicarbonat (Bleihydroxidcarbonat 2 PbCO3 × Pb(OH)2). Ein Überschuss an CO2 wandelt das gefällte Carbonat in das wasserlösliche BleihydrogencarbonatBleihydrogencarbonat um.
Verwendung
Blei(II)-carbonat ist Edukt bei der Herstellung veschiedener anderer Blei-Verbindungen; so resultiert beispielsweise aus der Reaktion mit einer Mineralsäure das entsprechende Bleisalz. In der Industrie fand die Chemikalie Anwendung als Katalysator bei der Polymerisierung von Formaldehyd zu Poly(oxymethylen) sowie als Hilfsstoff bei der Synthese von Chloropren.
Gefahren-Hinweise nach GHS
(Allgemeine Hinweise ohne Gewähr auf Richtigkeit und Vollständigkeit! Die Angaben ersetzen weder das Sicherheitsdatenblatt Chemikalien noch eine Gefährdungsbeurteilung, sondern geben eine allgemeine Übersicht hinsichtlich der Gefährdung durch den Gefahrstoff.)



Signalwort: Gefahr
Gefahrenhinweise (H-Sätze):
- H302
Gesundheitsschädlich bei Verschlucken. - H332
Gesundheitsschädlich bei Einatmen. - H360Df
Kann das Kind im Mutterleib schädigen. Kann vermutlich die Fruchtbarkeit beeinträchtigen. - H373
Kann die Organe schädigen bei längerer oder wiederholter Exposition. - H400
Sehr giftig für Wasserorganismen. - H410
Sehr giftig für Wasserorganismen, mit langfristiger Wirkung.
Zur Kennzeichnung in der EU siehe ECHA Substance Infocard 100.009.041 sowie Informationen zu REACh unter ECHA Chem 100.009.041.
Zur Toxikologie und zum Arbeitsschutz beim Umgang mit Bleicarbonat sowie Maßnahmen im Gefahrenfall siehe: Gefahrstoffinformationssystem GESTIS, ZVG-Nr. 004500.
Weitere unfangreiche toxikologische Daten und Gefahrstoff-Informationen liefert die Datenbank für gefährliche Stoffe (Hazardous Substances Data Bank) unter der Nummer HSDB 1649.
Internationales Sicherheitsdatenblatt (SDS, MSDS) siehe ICSC: 0999 [englisch].
Externe Informationsquellen
Hersteller und Bezugsquellen
In der nachfolgenden Tabelle sind Produzenten und Lieferanten von Bleicarbonat als kommerzielle Chemikalie für Labor, Forschung, Industrie und Produktion mit den entsprechenden Kontaktdaten verzeichnet.
Literatur und Quellen
[0] - Fach- und Forschungsartikel in wissenschaftlichen Zeitschriften via PubMed: "Lead carbonate".
[1] - Kurt Sahl:
Verfeinerung der Kristallstruktur von Cerussit, PbCO3.
In: Zeitschrift für Kristallographie, (1974), DOI 10.1524/zkri.1974.139.3-5.215.
Letzte Änderung am 16.02.2024.
Permalink: https://www.internetchemie.info/substanz/Bleicarbonat.php
© 1996 - 2026 Internetchemie ChemLin