Antimonwasserstoff ist eine anorganisch-chemische Verbindung aus Antimon in der dreiwertigen Form und Wasserstoff, die häufig auch Stibin oder Stiban genannt wird. Die Chemikalie ist ein einkerniges Stammhydrid; die konjugierte Base SbH4+ ist das Stibonium-Ion. Die Antimon-Verbindung wird der Gruppe der anorganischen Hydride bzw. den Pniktogenhydriden zugeordnet.
Bezeichnungen und Identifikatoren
Antimonwasserstoff
H3Sb
SbH3
124,784 (g/mol)
7803-52-3
620-578-3
OUULRIDHGPHMNQ-UHFFFAOYSA-N
Systematischer Name
Stiban
Weitere Bezeichnungen, Synonyme
Stibin; Antimonhydrid; Antimontrihydrid; Monostiban; Trihydridoantimon; Wasserstoffantimonid
Englische Bezeichnung
Stibine
Stibane; Trihydridoantimony; Antimony trihydride; Hydrogen antimonide
Chemische Formeln
Brutto- bzw. Summenformel und Strukturformel der chemischen Verbindung Antimonwasserstoff:
H3Sb oder SbH3
Mr = 124,784 g/mol
Stiban
SMILES: [SbH3]
Daten und Eigenschaften
Übersicht über die (bekannten) chemischen und physikalischen Eigenschaften: Antimonwasserstoff. Es gelten - soweit nicht anders angegeben - Raumumgebungsbedingungen (Normaldruck, 0 % Luftfeuchtigkeit, 20 °C).
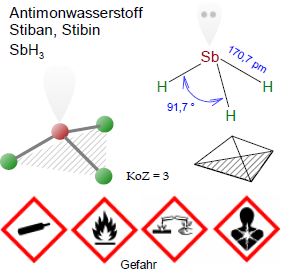
Unter Standardbedingungen erscheint Antimonwasserstoff als farbloses Gas mit stechendem, unangenehmem, H2S-ähnlichem Geruch. Die Substanz zersetzt sich langsam beim Stehen bei Raumtemperatur; die Zersetzungsprodukte sind Wasserstoff und metallisches Sb, das sich meist in Form eines Antimon-Spiegels niederschlägt. Das Stiban Molekül ist trigonal pyramidenförmig aufgebaut mit H-Sb-H-Winkeln von 91,7 ° und Sb-H-Abständen von 170,7 pm (1,707 Å).
-88,5 °C
-17 °C
2,16 g cm-1 bei -17 °C
5,4 g/L (Gas)
82,8 kPa bei -23 °C
145,11 kJ/mol bei 20 °C
148 kJ/mol
0,041 kJ/(mol K)
0,4 × 10-30 C m
9,51 eV
Prozentuale und isotopische Zusammensetzung:
Massenbezogene elementare Zusammensetzung und Isotopen-Anteile der Verbindung Antimonwasserstoff - H3Sb - berechnet auf Grundlage der Molekülmasse.
.Element E
der Atome Ex
und der Isotope *
der Isotope
Ex an Formelmasse
Wasserstoff
ΣAr = 3,024 u
1H: 1,00783 u [99,99 %]
2H: 2,0141 u [0,01 %]
3H: 3,01605 u [<< 1 %]
1H: 2,42315 %
2H: 0,00024 %
3H: Spuren
Antimon
121Sb: 120,90381 u [57,21 %]
123Sb: 122,90421 u [42,79 %]
121Sb: 55,82358 %
123Sb: 41,75303 %
*) Die dritte Spalte führt die Atommassen bzw. Isotopenmassen der beteligten Elemente sowie - in eckigen Klammern - die natürliche Isotopenzusammensetzung auf.
Weitere berechnete Daten
Die molare Masse ist M = 124,784 Gramm pro Mol.
Die Stoffmenge von einem Kilogramm der Substanz ist n = 8,014 mol.
Die Stoffmenge von einem Gramm der Substanz ist n = 0,008 mol.
Monoisotopische Masse: 123,9272850966 Da - bezogen auf 1H3121Sb.
Synthese, Gewinnung
Antimonwasserstoff kann generell durch die chemische Reaktion von Metallantimoniden mit Säure, die chemische Reduktion von Antimonverbindungen und durch die Elektrolyse von sauren oder alkalischen Lösungen unter Verwendung einer metallischen Antimonkathode hergestellt werden. Möglich ist auch das Auflösen einer Zink-Antimon- oder Magnesium-Antimon-Legierung in verdünnter Salzsäure bzw. die Einwirkung von naszierendem Wasserstoff auf in Wasser gelöste Sb-Verbindungen.
Verwendung
Hochreines Stiban wird als n-Typ-Gasphasen-Dotierungsmittel für Silicium in Halbleitern verwendet.
Gefahren-Hinweise nach GHS
(Allgemeine Hinweise ohne Gewähr auf Richtigkeit und Vollständigkeit! Die Angaben ersetzen weder das Sicherheitsdatenblatt Chemikalien noch eine Gefährdungsbeurteilung, sondern geben eine allgemeine Übersicht hinsichtlich der Gefährdung durch den Gefahrstoff.)



Signalwort: Gefahr
Gefahrenhinweise (H-Sätze):
- H220
Extrem entzündbares Gas. - H280
Enthält Gas unter Druck; kann bei Erwärmung explodieren. - H330
Lebensgefahr bei Einatmen. - H370
Schädigt die Organe.
Zur Kennzeichnung in der EU siehe ECHA Substance Infocard 100.149.507 sowie Informationen zu REACh unter ECHA Chem 100.149.507.
Zur Toxikologie und zum Arbeitsschutz beim Umgang mit Antimonwasserstoff sowie Maßnahmen im Gefahrenfall siehe: Gefahrstoffinformationssystem GESTIS, ZVG-Nr. 041070.
Externe Informationsquellen
Hersteller und Bezugsquellen
In der nachfolgenden Tabelle sind Produzenten und Lieferanten von Antimonwasserstoff als kommerzielle Chemikalie für Labor, Forschung, Industrie und Produktion mit den entsprechenden Kontaktdaten verzeichnet.
Letzte Änderung am 12.02.2024.
Permalink: https://www.internetchemie.info/substanz/Antimonwasserstoff.php
© 1996 - 2026 Internetchemie ChemLin