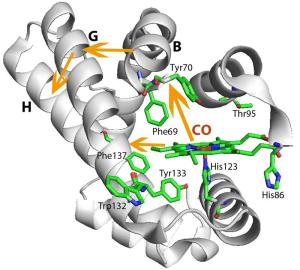
Wie genau einzellige Organismen wie Bakterien es schaffen, auf ihre Umwelt zu reagieren, ist nicht vollkommen verstanden.
Neue Erkenntnisse hat Dr. Samir El-Mashtoly vom RUB-Lehrstuhl Biophysik, geleitet von Prof. Dr. Klaus Gerwert, zusammen mit Kollegen aus Japan gewonnen.
Im Journal of Biological Chemistry beschreiben die Forscher die molekularen Interaktionen im Bakterium Bacillus subtilis während der Aerotaxis, also der Änderung in der Bewegungsrichtung abhängig von der Sauerstoffkonzentration in der Umgebung.
Das Team untersuchte strukturelle Änderungen des Proteins HemAT. Über eine Signalkette sendet es Kommandos an den Motor der Schwimmgeißel des Bakteriums.
Signalübertragungskette
Zunächst bindet Sauerstoff an die Häm-Gruppe von HemAT; diese Gruppe ist auch aus dem Hämoglobin roter Blutkörperchen bekannt und wird als "sensorische Domäne" von HemAT bezeichnet. Durch die Bindung ändert sich die Struktur der sensorischen Domäne. Das löst weitere strukturelle Veränderungen in HemAT aus, die letztendlich die Signal-Domäne des Proteins erreichen. Die Signal-Domäne überträgt dann die Information über die steigende Sauerstoffkonzentration an weitere Proteine in der Zelle. Diese Proteine leiten die Botschaft an den Motor der Schwimmgeißel weiter. Das Forscherteam untersuchte, wie die Information innerhalb von HemAT von der sensorischen Domäne zur Signal-Domäne wandert.
Proteinhelices übermitteln die Botschaft
Zu diesem Zweck nutzte Dr. El-Mashtoly die Einrichtung für zeitaufgelöste Ultraviolett-Resonanz-Raman-Spektroskopie am Picobiology Institute in Japan. Mit dieser Methode lassen sich zum Beispiel strukturelle Informationen über das Protein und Interaktionen von Wasserstoffbrückenbindungen verfolgen - auf einer Nano- bis Mikrosekunden-Zeitskala. Die Ergebnisse legen nahe, dass die strukturellen Änderungen in der sensorischen Domäne, also der Häm-Gruppe, zwei Proteinhelices in HemAT verschieben. Diese Verschiebung beeinflusst eine weitere Helix, die bis in die Signal-Domäne hineinragt. Über eine Serie von strukturellen Änderungen erreicht also die Information über die Sauerstoffbindung die Signal-Domäne.
Zusatzinformationen:
Samir F. El-Mashtoly, Minoru Kubo, Yuzong Gu, Hitomi Sawai, Satoru Nakashima, Takashi Ogura, Shigetoshi Aono, Teizo Kitagawa:
Site-specific Protein Dynamics in Communication Pathway from Sensor to Signaling Domain of Oxygen Sensor Protein, HemAT-Bs.
In: The Journal of Biological Chemistry; 287, 19973 - 19984, 08. Juni 2012, DOI 10.1074/jbc.M112.357855
Quelle: Ruhr-Universität Bochum, RUB
Aktualisiert am 26.06.2012.
Permalink: https://www.internetchemie.info/news/2012/jun12/bakterien-aerotaxis.php
© 1996 - 2026 Internetchemie ChemLin