Fossile Rohstoffe gehen zur Neige und ihre Verwendung setzt das Treibhausgas Kohlendioxid (CO2) frei.
Beide Probleme ließen sich deutlich abschwächen, wenn man Kohlendioxid als Kohlenstoffquelle für die Herstellung von Kraftstoffen und Chemie-Rohstoffen nutzen könnte.
Deutsche Forscher stellten in der Zeitschrift Angewandte Chemie nun erstmals die Möglichkeit vor, die mehrstufige Umwandlung von CO2 zu Methanol (CH3OH) mit einem homogenen Übergangsmetall-Katalysator in Lösung durchzuführen.
Methanol und seine Folgeprodukte können nicht nur in klassischen Verbrennungsmotoren oder Brennstoffzellen genutzt werden, sondern stellen auch einen vielseitigen Rohstoff für die chemische Industrie dar. Das bisher etablierte großtechnische Verfahren zur Herstellung von Methanol basiert auf Synthesegas, einer aus fossilen Ressourcen gewonnenen Mischung aus Wasserstoff und Kohlenmonoxid. Das Verfahren nutzt dabei unter hohem Druck und hoher Temperatur einen heterogenen Katalysator, welcher als Feststoff in einer anderen Phase vorliegt als die gasförmigen oder flüssigen Edukte und Produkte.
Inzwischen gibt es eine Reihe von neuartigen Ansätzen, Kohlendioxid als Ausgansstoff für die Herstellung von Methanol zu nutzen. Die große Herausforderung für die Katalyseforschung besteht darin, nicht nur das sehr stabile CO2-Molekül zu aktivieren, sondern auch die komplexe mehrstufige Umsetzung zu Methanol zu katalysieren. Maßgeschneiderte Katalysatoren sind der Schlüssel, um die Aktivierung dieses wenig reaktiven C1-Bausteins zu ermöglichen.
Wissenschaftler am Institut für Technische und Makromolekulare Chemie der RWTH Aachen verfolgen einen neuen Ansatz, um Methanol durch Reduktion von CO2 mit elementarem Wasserstoff zu gewinnen. Während die meisten bisherigen Verfahren heterogen-katalytisch laufen, handelt es sich hier um ein homogen-katalytisches Verfahren: Katalysator und Edukte liegen in Lösung, also in derselben Phase vor. Homogene Übergangsmetall-Katalysatoren kommen häufig mit milderen Reaktionsbedingungen aus und die gezielte Entwicklung des Katalysators ermöglicht oft höhere Selektivitäten. Bislang war jedoch kein homogener Metallkomplex bekannt, der die über mehrere Zwischenstufen verlaufende Bildung von Methanol aus Kohlendioxid und Wasserstoff katalysieren konnte.
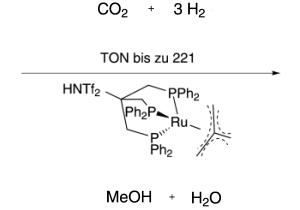
Das Team um Jürgen Klankermayer und Walter Leitner hat nun für diese komplexe Umsetzung einen maßgeschneiderten homogenen Katalysator, einen speziellen Ruthenium-Phosphin-Komplex, entwickelt. Der in einem Lösungsmittel, im einfachsten Fall Methanol selbst, gelöste Katalysator wird in einem Autoklaven unter Druck mit Kohlendioxid und Wasserstoff versetzt. Daraufhin verknüpft er schrittweise ein Molekül CO2 mit drei Molekülen Wasserstoff unter Bildung von Methanol und Wasser.
"Das ist das erste Beispiel einer Hydrierung von CO2 zu Methanol unter Verwendung eines molekular definierten Katalysators unter relativ milden Reaktionsbedingungen", erläutern Leitner und Klankermayer. "Nun erforschen wir, wie die Reaktion im Detail abläuft, um den Katalysator weiterzuentwickeln."
Über den Autor
Dr. Jürgen Klankermayer ist Professor am Institut für Technische Chemie und Makromolekulare Chemie (ITMC) der RWTH Aachen, wo er die Arbeitsgruppe "Mechanismen in der Katalyse" leitet. Seine Forschungsschwerpunkte liegen auf den Gebieten Mechanismen der Katalyse, NMR-spektroskopische Methoden in der Katalyse, Asymmetrische Katalyse, Anwendung ionischer Flüssigkeiten in der Katalyse, Kraftstoffe und Chemikalien aus Biomasse sowie nachhaltige industrielle Chemie.
Zusatzinformationen:
Sebastian Wesselbaum, Thorsten vom Stein, Prof. Dr. Jürgen Klankermayer, Prof. Dr. Walter Leitner:
Hydrogenation of Carbon Dioxide to Methanol by Using a Homogeneous Ruthenium-Phosphine Catalyst.
In: Angewandte Chemie; Volume 124, Issue 30, 7617-7620, online veröffentlicht am 15. Juni 2012, DOI 10.1002/ange.201202320
Quelle: Angewandte Chemie, Presseinformation Nr. 26/2012
Aktualisiert am 18.07.2012.
Permalink: https://www.internetchemie.info/news/2012/jul12/kohlendioxid-methanol-hydrierung.php
© 1996 - 2026 Internetchemie ChemLin